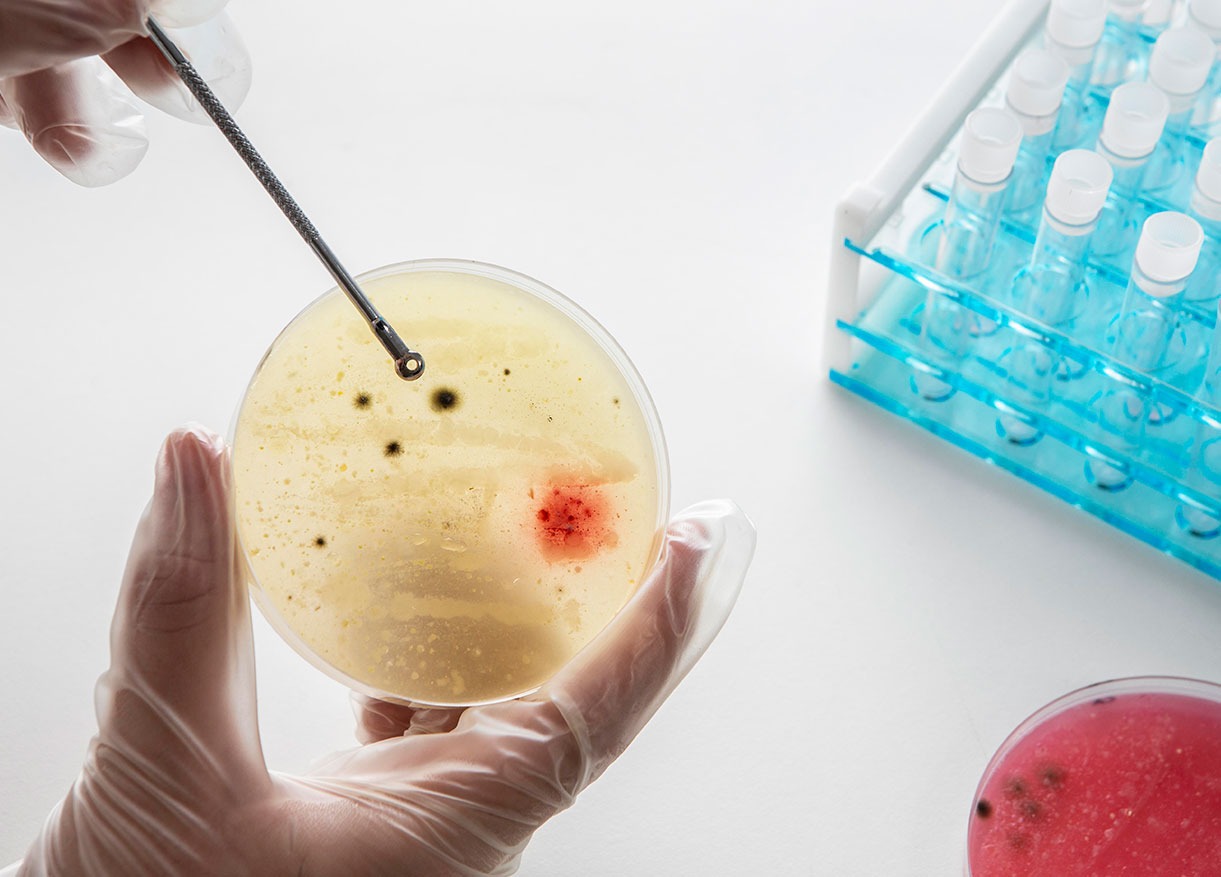
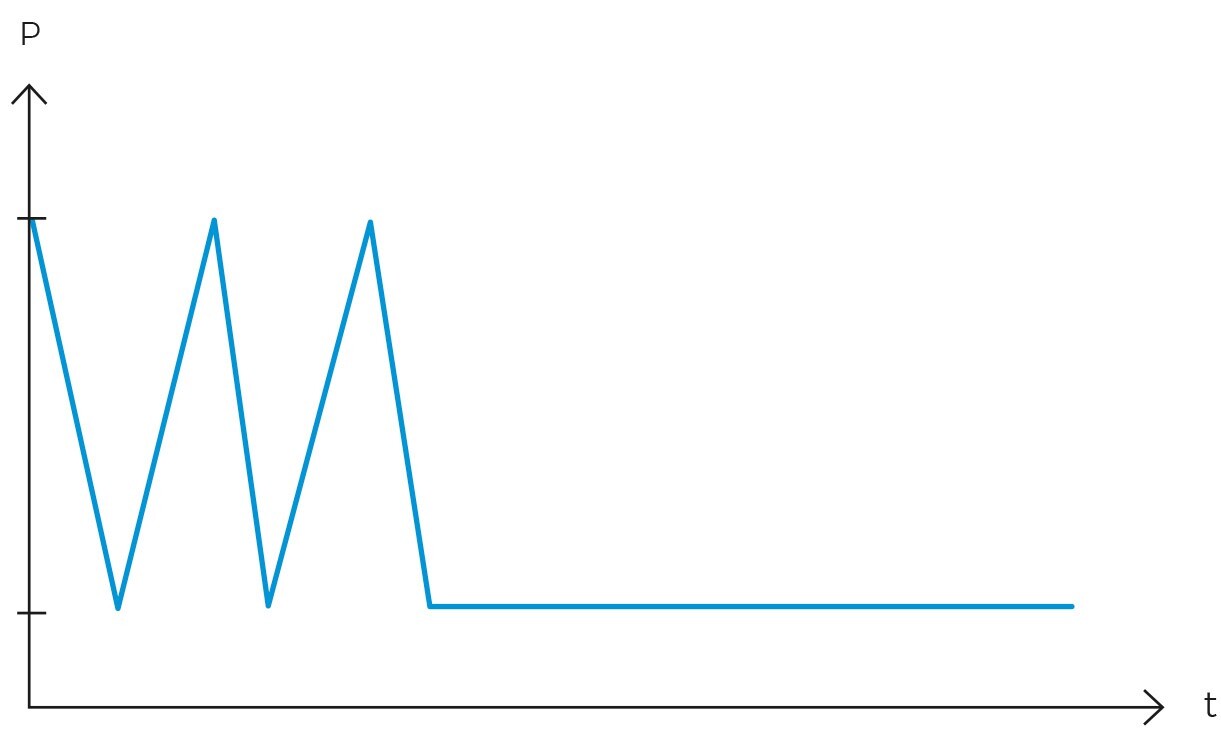
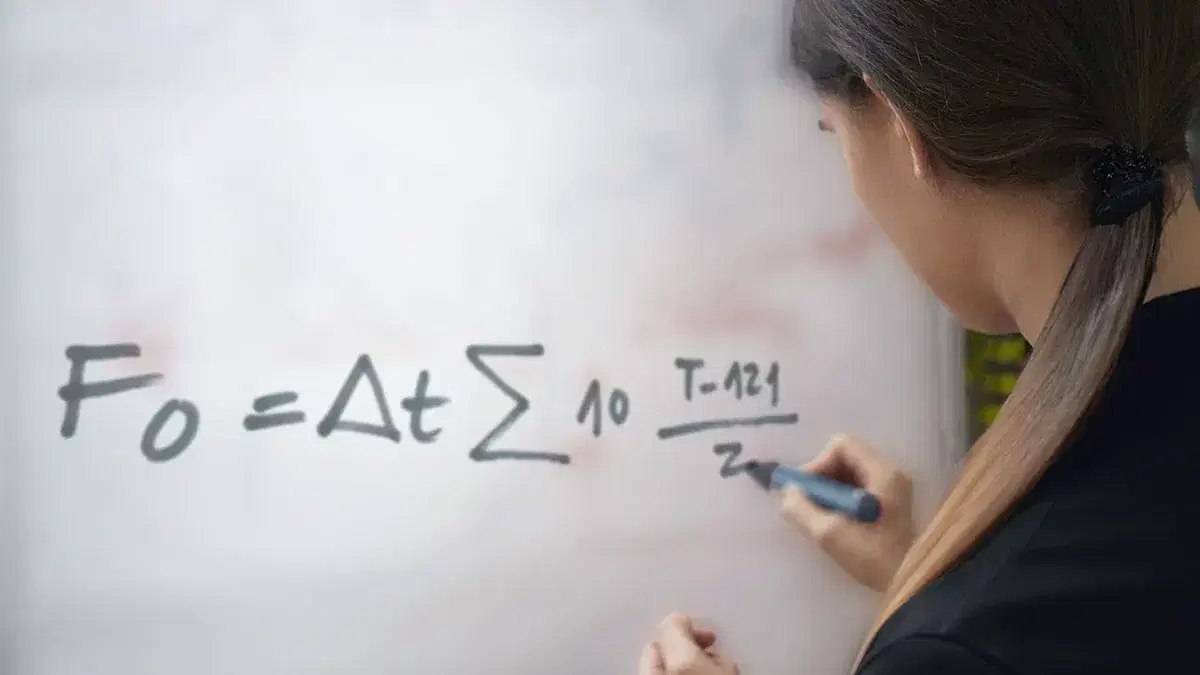La sterilizzazione dei liquidi in autoclave è una procedura comune nei laboratori di microbiologia e nei centri di ricerca, dove la sterilità dei liquidi è essenziale per l’integrità degli esperimenti scientifici e dei processi produttivi.
Le autoclavi, dispositivi che funzionano con vapore acqueo pressurizzato, sono comunemente utilizzate per sterilizzare sia strumenti che oggetti solidi. Tuttavia, la sterilizzazione dei liquidi, come i terreni di coltura e le soluzioni tampone, presenta sfide uniche che influenzano la progettazione e la durata del ciclo di sterilizzazione da impiegare.
Un aspetto critico della sterilizzazione dei liquidi è evitare l’effetto “boil-over”, un fenomeno che si verifica quando un liquido caldo in un contenitore chiuso subisce un’improvvisa variazione di pressione, causando l’ebollizione spontanea e la fuoriuscita. Questo rischio, insieme alla necessità di controllare attentamente la velocità di riscaldamento e raffreddamento, distingue la sterilizzazione di carichi liquidi da quella di oggetti solidi.
Principi fondamentali del ciclo di liquidi in autoclave
Il ciclo di liquidi in un’autoclave si basa su un ciclo a gravità con alcune modifiche, in quanto la fase di raffreddamento deve essere controllata e la durata della fase di riscaldamento deve essere prolungata. Sebbene la temperatura di sterilizzazione utilizzata sia di 121°C, la durata dipenderà in larga misura dalla quantità di liquidi e dalle dimensioni dei contenitori.
A differenza dei cicli a gravità e di vuoto, che sono destinati ai processi di sterilizzazione di materiali solidi e porosi, il ciclo di liquidi è progettato specificamente per trattare carichi liquidi in contenitori e mira a evitare i fallimenti della sterilizzazione, il surriscaldamento del carico, l’ebollizione spontanea e a ridurre al minimo la perdita per evaporazione.

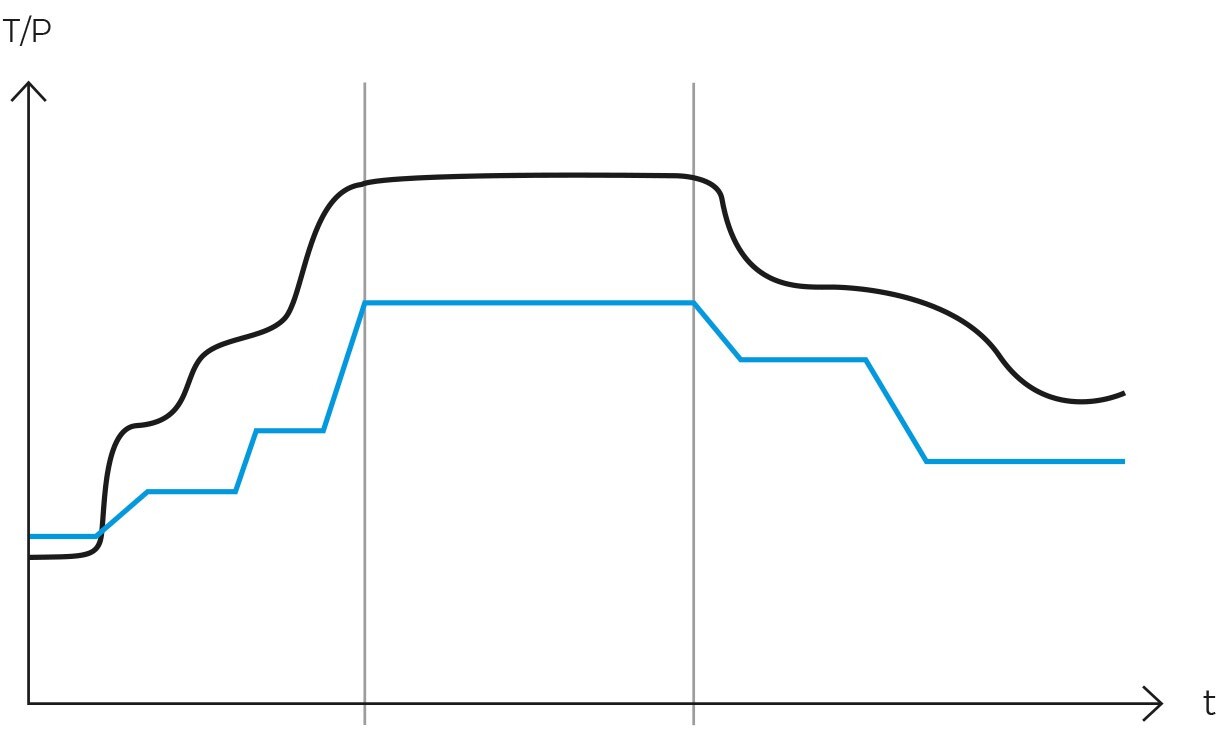
Per raggiungere questi obiettivi, è fondamentale un controllo preciso della fase di riscaldamento. Grandi volumi di liquidi richiedono molto tempo per riscaldarsi, in quanto subiscono un ritardo significativo nel portare la loro temperatura a quella della camera, quindi se applichiamo lo stesso tempo di esposizione di un ciclo di solidi per sterilizzare un carico liquido, vedremo che il carico liquido non raggiungerà la temperatura di sterilizzazione alla stessa velocità.
L’effetto opposto si verifica nella fase di raffreddamento: i liquidi impiegano molto più tempo a raffreddarsi, per cui gli utenti inesperti corrono il rischio di ustioni quando rimuovono il carico, perché anche se la camera si è raffreddata fino a raggiungere una temperatura sicura, i liquidi possono essere ancora molto caldi.
Un altro aspetto da tenere in considerazione è che una depressurizzazione troppo rapida durante la fase di raffreddamento può causare l’effetto “boil-over”, cioè l’ebollizione spontanea del liquido. Pertanto, il ciclo di liquidi deve depressurizzare la camera in modo graduale, riducendo lentamente la pressione per evitare improvvisi cambiamenti di temperatura.
Sfide uniche della sterilizzazione dei liquidi
Come abbiamo visto, la sterilizzazione dei liquidi in autoclave affronta sfide specifiche dovute alle proprietà fisiche dei liquidi e alla necessità di mantenere la loro integrità durante il processo.
Gestire l’elevato calore specifico dei liquidi
Una delle sfide principali nella sterilizzazione dei liquidi è il loro elevato calore specifico. I liquidi, rispetto ai solidi, richiedono molta più energia per aumentare la loro temperatura. Ciò significa che i cicli di sterilizzazione dei liquidi devono essere più lunghi, in quanto il liquido impiega più tempo per raggiungere la temperatura di sterilizzazione. Allo stesso modo, anche il raffreddamento richiede più tempo, prolungando la durata complessiva del ciclo.
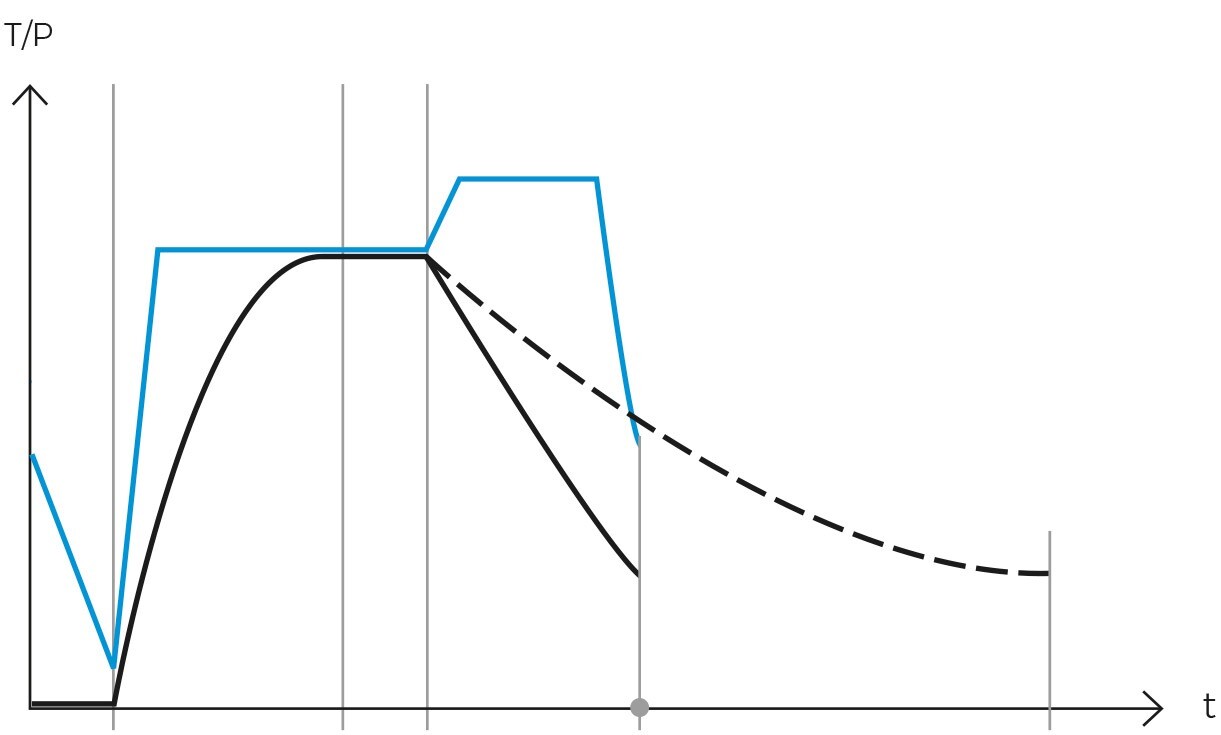
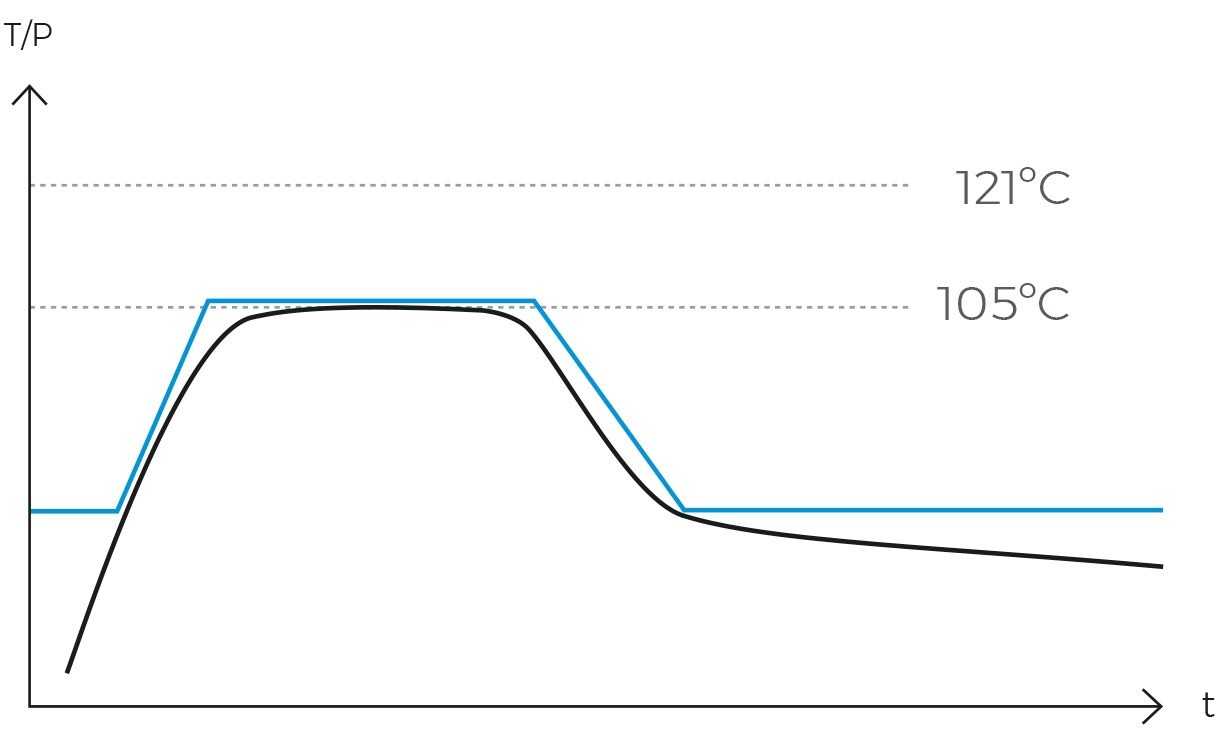
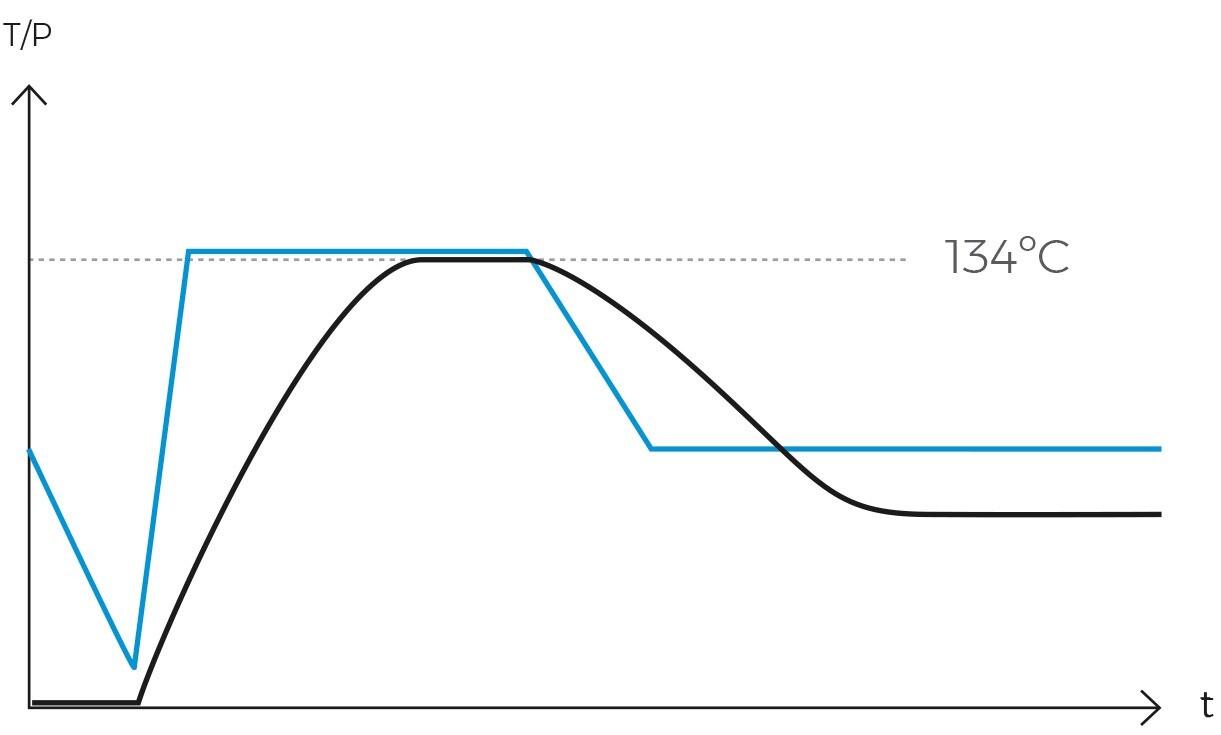
Per risolvere questo problema, le autoclavi moderne possono essere dotate di una sonda centrale che monitora la temperatura interna del carico e agisce anche da regolatore del ciclo. Ciò significa che se programmiamo un ciclo di liquidi con una temperatura di sterilizzazione di 119°C per 10 minuti, il timer non si avvierà fino a quando la temperatura del carico non avrà raggiunto i 119°C.
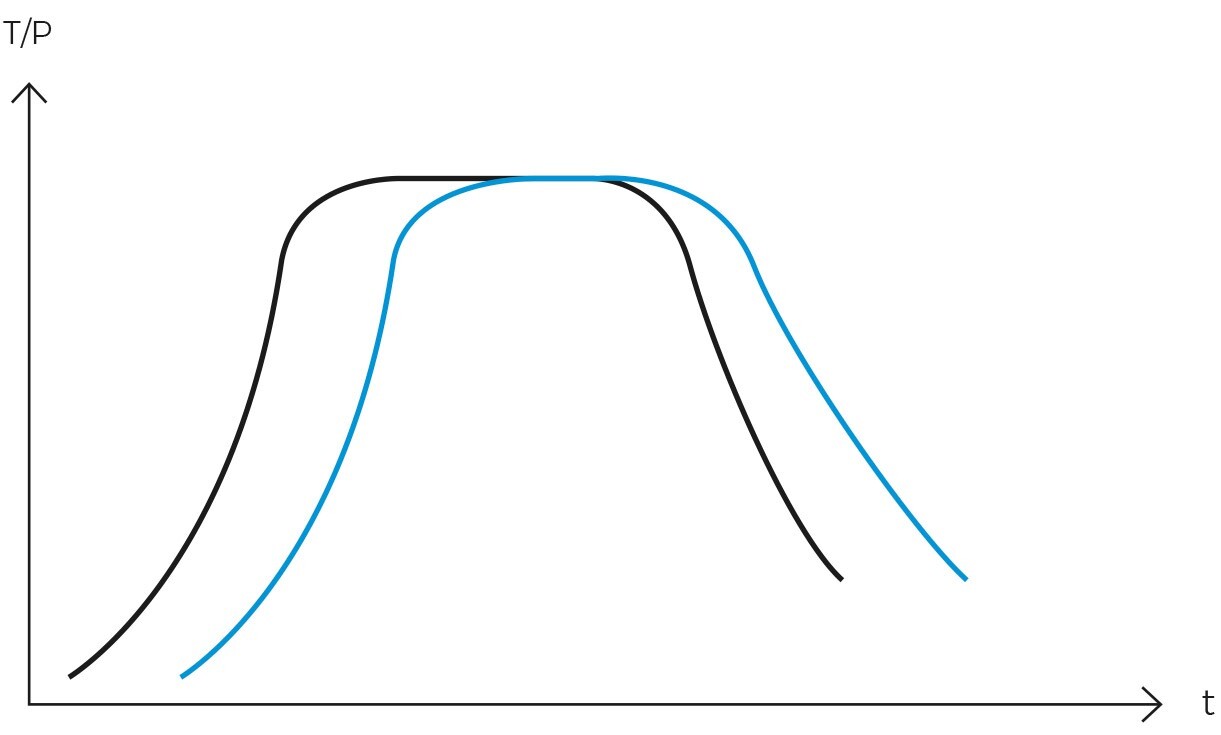
Nelle autoclavi tradizionali, il timer si avvia quando la temperatura della camera raggiunge i 119°C, ma la temperatura del carico può essere anche di 105°C. Questa discrepanza è una causa comune della mancata sterilizzazione corretta dei carichi liquidi.
Prevenzione dell’effetto “boil-over”
Questo fenomeno, chiamato anche ebollizione rapida, è causato da un rapido cambiamento di pressione durante la fase di raffreddamento, che può provocare schizzi e fuoriuscite, con conseguente perdita di carico sterilizzato e, peggio ancora, imbrattamento di attrezzature e del resto del carico.
A nessuno piace dover pulire un’autoclave con residui di agar solidificati sulle pareti della camera. Per evitare questo problema, è necessaria una depressurizzazione scaglionata durante la fase di raffreddamento e un monitoraggio preciso della temperatura di carico mediante una sonda centrale.
Mantenere l’integrità del liquido
Un’altra sfida importante è quella di mantenere l’integrità chimica e biologica dei liquidi, soprattutto perché richiedono molto tempo per raffreddarsi, il che comporta una cottura eccessiva e una notevole perdita di tempo. Questa situazione è particolarmente problematica per i liquidi termolabili, le cui proprietà possono essere influenzate negativamente da un’esposizione non necessaria ad alte temperature. Ad esempio, alcuni terreni di coltura vedono peggiorare il loro tasso di fertilità a causa della scomposizione delle proteine o dei trigliceridi, mentre alcuni reagenti possono subire cambiamenti nella loro composizione chimica.
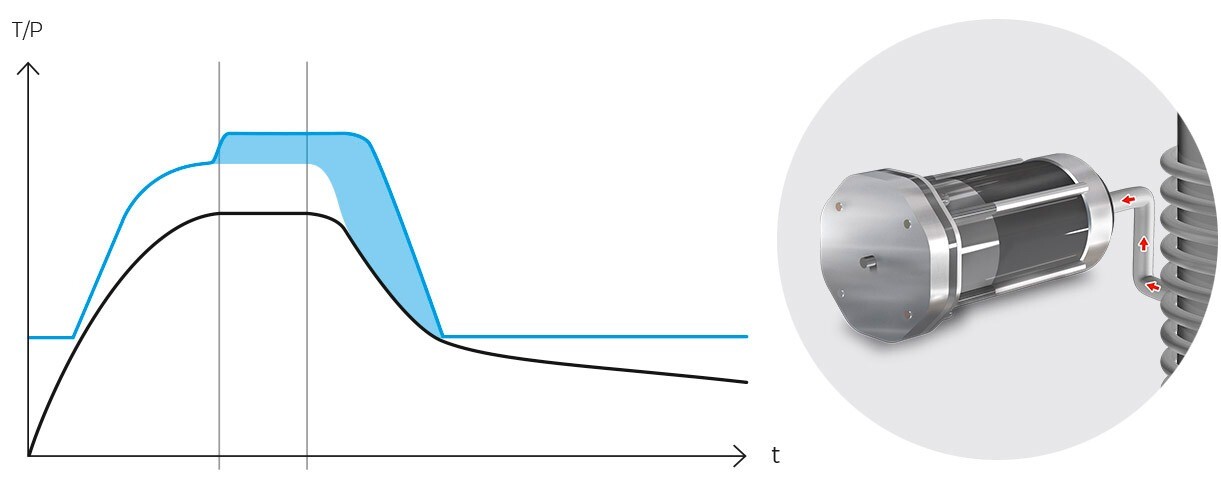
Per combattere questo problema e migliorare la produttività del laboratorio, si raccomanda l’uso di autoclavi con sistemi di raffreddamento rapido, che riducono significativamente il tempo di esposizione al calore e consentono un recupero molto più rapido del carico, aumentando drasticamente la produttività del laboratorio. A seconda del tipo di sistema di raffreddamento rapido utilizzato e del tipo di carico, si possono ottenere riduzioni fino al 90%, il che rappresenta un risparmio di oltre 60 minuti in ogni ciclo di sterilizzazione.
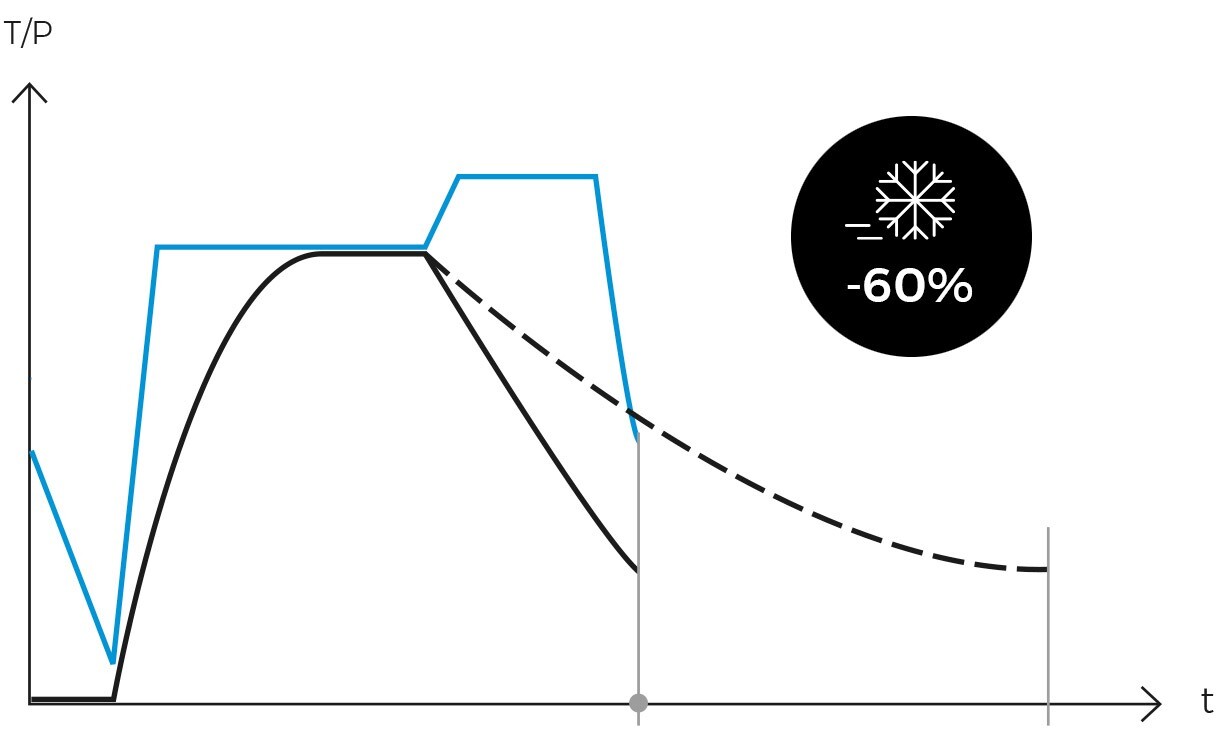
Tra le tecnologie più comuni ci sono le ventole e le serpentine ad acqua. Inoltre, le autoclavi più moderne includono sistemi di sovrapressione per evitare il “boil-over” durante la fase di raffreddamento e per ridurre al minimo la perdita di liquido per evaporazione. Un altro tipo di autoclavi, i preparatori di terreni, consentono di ottenere riduzioni ancora più rapide.
Parametri chiave del ciclo di liquidi
È chiaro che il ciclo di liquidi in un’autoclave è un processo delicato che richiede l’impostazione precisa di diversi parametri per garantire una sterilizzazione efficace e sicura. Questi parametri includono la temperatura della camera, la temperatura del carico, la pressione della camera, il tempo di esposizione e il controllo della fase di raffreddamento, ognuno dei quali svolge un ruolo cruciale per il successo del processo.
-
Temperatura e pressione ottimali
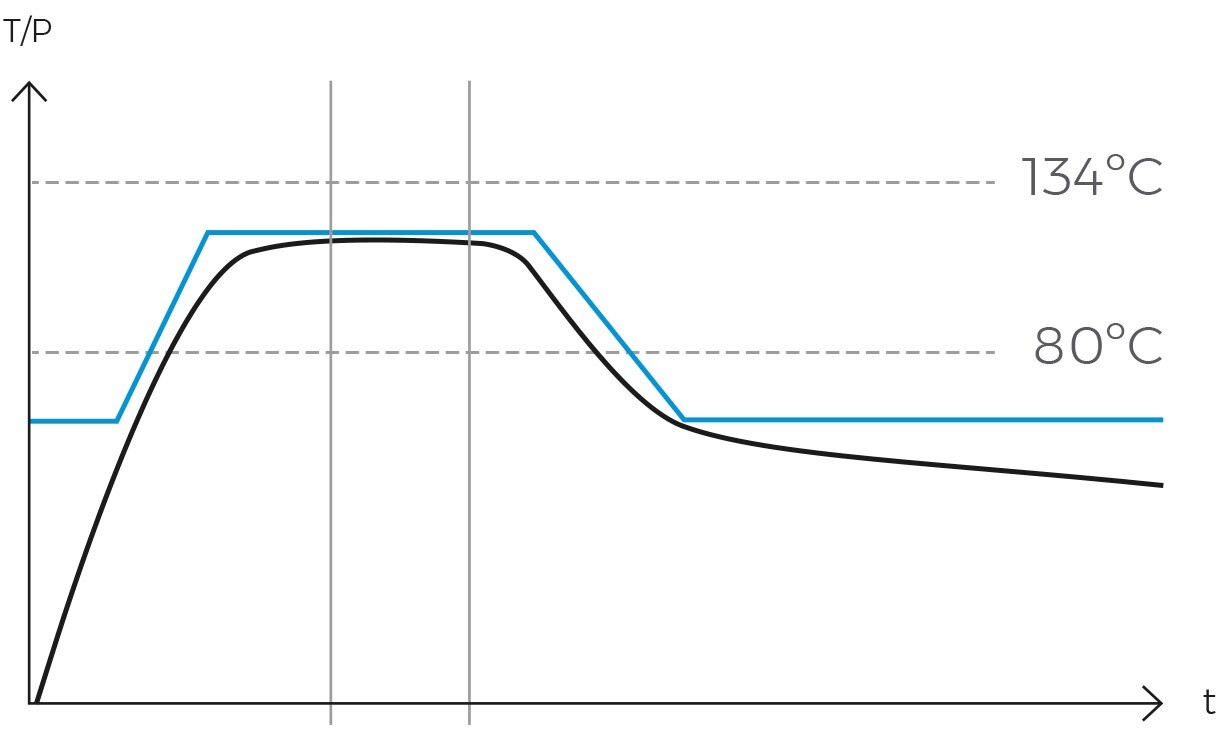
La temperatura e la pressione sono i fattori più critici nella sterilizzazione dei liquidi. In genere, i liquidi vengono sterilizzati ad una temperatura di circa 121°C, ottenuta ad una pressione di circa 1,1 barg. Questa combinazione di temperatura e pressione elevate è efficace per uccidere qualsiasi microrganismo, comprese le spore. Tuttavia, per i liquidi termolabili, è necessario utilizzare temperature più basse.
In ogni caso, è essenziale mantenere costantemente queste condizioni durante la fase di sterilizzazione per garantire la completa sterilità del liquido. È inoltre consigliabile utilizzare sempre una sonda centrale che monitori la temperatura del carico e che sia questa a governare il ciclo piuttosto che la temperatura della camera.
-
Tempo di sterilizzazione
Il tempo di esposizione alla temperatura di sterilizzazione è un altro parametro fondamentale. Questo tempo varia in base al tipo e al volume del liquido, nonché al carico totale dell’autoclave. I liquidi richiedono un tempo di esposizione più lungo rispetto ai solidi, a causa del loro calore specifico più elevato.
I tempi di esposizione tipici possono variare da 15 a più di 30 minuti, a seconda di questi fattori. Due raccomandazioni da considerare sono l’utilizzo di indicatori biologici per convalidare i processi e il tentativo di ridurre al minimo il volume dei contenitori, in modo che i tempi di ciclo siano più brevi. È più efficace trattare più contenitori di volume ridotto che meno contenitori di volume maggiore.
Infine, si raccomanda l’uso di cicli di sterilizzazione regolati in base all’F₀ per la sua capacità di quantificare con precisione la letalità di un processo di sterilizzazione. Utilizzando il valore F₀, il ciclo di sterilizzazione viene regolato automaticamente in base alle esigenze specifiche del carico. In questo modo si evitano errori di inefficienza dovuti a esposizioni troppo brevi e problemi di coerenza legati alla disposizione del carico all’interno dell’autoclave, sia in termini di forma che di numero di contenitori.
-
Controllo della fase di raffreddamento
La fase di raffreddamento è una fase importante del ciclo di liquidi. Una depressurizzazione rapida causerà un’ebollizione incontrollata del carico liquido, mentre un raffreddamento troppo lento prolungherà inutilmente il ciclo e cuocerà eccessivamente il carico, riducendo la qualità del liquido trattato. Pertanto, è necessario utilizzare un’autoclave con un programma per liquidi, per evitare cambiamenti improvvisi di temperatura e pressione durante la fase di raffreddamento.
Per i laboratori con richieste di volumi elevati si consiglia di utilizzare autoclavi con sistema di raffreddamento rapido o preparatori di terreni per accelerare questo processo senza comprometterne la sicurezza o l’efficacia. Grazie a questo tipo di autoclavi, la produttività del laboratorio può essere migliorata in modo esponenziale.
-
Monitoraggio e convalida
Il monitoraggio e la registrazione di ogni processo sono essenziali per garantire che ogni ciclo di sterilizzazione venga eseguito correttamente. Di solito questo si ottiene attraverso sensori e controlli automatizzati che regolano la temperatura, la pressione e il tempo, come necessario. Inoltre, la convalida periodica del buon funzionamento dell’autoclave è fondamentale per confermare che le sue prestazioni rimangano efficaci nel tempo.
Autoclavi e accessori specifici per la sterilizzazione dei liquidi
Sul mercato sono disponibili diverse opzioni per migliorare l’efficienza e la sicurezza della sterilizzazione dei liquidi, tutte basate sull’uso di tecnologie e modelli specializzati:
-
Autoclavi dotate di cicli per liquidi
Queste autoclavi sono dotate di sistemi di controllo e di programmi specifici per la sterilizzazione dei liquidi. I modelli più avanzati consentono persino la programmazione in base al valore F₀ anziché alla temperatura di sterilizzazione.
-
Autoclavi con sonda flessibile centrale
Forniscono letture della temperatura in tempo reale delle condizioni all’interno del carico liquido. Questo accessorio permette di controllare che la sterilizzazione sia eseguita correttamente e che il carico sia esposto alla temperatura target per il tempo richiesto.

-
Sistemi di raffreddamento rapido
Questi sistemi consentono di ridurre la durata della fase di raffreddamento. Esempi includono l’uso di ventole esterne, ventole interne, una serpentina ad acqua, una camicia di raffreddamento o sistemi di docce d’acqua.
Considerazioni speciali per i carichi liquidi sensibili al calore
La sterilizzazione dei carichi liquidi termolabili richiede un approccio più attento e personalizzato per preservare l’integrità fisica e chimica del carico, garantendone al contempo la sterilità. Tali carichi liquidi, come alcuni reagenti chimici e terreni di coltura, possono degradarsi o alterare le loro proprietà se esposti ad alte temperature per troppo tempo.
Per evitare questo problema, è consigliabile lavorare con l’equivalenza termica tra temperature e tempi diversi, utilizzando il valore F₀.
Utilizzo del valore F₀
Il valore F₀ consente di quantificare la sterilità di un processo termico e l’equivalenza della letalità tra due processi. È un metodo ampiamente utilizzato nella sterilizzazione degli alimenti ed è anche essenziale per preservare l’integrità delle sostanze soggette a termolisi.
In particolare, il valore F₀ rappresenta il tempo di esposizione in minuti equivalente a 121°C. Quindi, un F₀ di 3 indica una sterilizzazione equivalente a tre minuti a 121°C. Continuando con l’esempio, applicando la formula, possiamo calcolare che un F₀ di 3 equivale a 6 minuti a 118°C. In altre parole, la sterilizzazione di 3 minuti a 121°C equivale alla sterilizzazione di 6 minuti a 118°C.
Fondamentalmente, consente di estrapolare l’efficacia sterilizzante di un processo ad altre temperature, facilitando l’adattamento preciso di un processo termico tramite la modifica della temperatura massima del processo, con l’obiettivo di poter ottimizzare il rapporto tra sterilizzazione e conservazione delle proprietà fisico-chimiche del prodotto.
Calcolo della durata di un ciclo regolato dai valori F₀
Quando si lavora con un’autoclave con programmi F₀, è necessario segnalare solo il valore F₀ target e la temperatura massima del processo, eliminando la necessità di programmare un tempo nel ciclo di sterilizzazione. In questo modo, l’autoclave misura automaticamente l’evoluzione del valore F₀ effettivo e arresta il ciclo quando viene raggiunto il valore F₀ target.
Raffreddamento di liquidi termolabili
Un raffreddamento accurato è altrettanto importante per i liquidi sensibili al calore. Un raffreddamento troppo lento può causare una sovraesposizione al calore. Allo stesso modo, una depressurizzazione rapida può provocare schizzi e fuoriuscite. Pertanto, si raccomanda vivamente di utilizzare autoclavi dotate di sistemi di raffreddamento rapido e di supporto della pressione per trattare questi tipi di carichi, in modo da ridurre al minimo necessario il tempo in cui il carico resta caldo.
Buone prassi e consigli per una sterilizzazione efficace dei liquidi in autoclave
Per ottimizzare la sterilizzazione dei liquidi in autoclave, consigliamo di seguire alcune pratiche:
-
Scelta corretta dei contenitori
Utilizza sempre contenitori resistenti al calore e lascia sempre uno spazio per l’espansione termica dei liquidi.
-
Contenitori con tappi sempre semiaperti
Per evitare la rottura dei contenitori o eventuali fuoriuscite, i liquidi non devono mai essere sterilizzati in contenitori ermetici, a meno che non si utilizzi un ciclo con supporto di pressione. Ad esempio, i tappi delle bottiglie devono essere leggermente svitati e le beute devono essere coperte con un foglio di alluminio.
-
Impostazione corretta dei parametri dell’autoclave
Regolare la durata del ciclo in base al volume totale dei contenitori da sterilizzare e affidarsi a un’autoclave che esegua una depressurizzazione scaglionata durante la fase di raffreddamento.
-
Utilizzare autoclavi con programmi per liquidi e un sistema di raffreddamento rapido.
In questo modo si risparmierà molto tempo, si eviterà una cottura eccessiva del carico, si offrirà una maggiore sicurezza agli operatori e, a lungo termine, si risparmierà molto tempo di pulizia necessaria a causa della fuoriuscita del carico.

-
Monitoraggio e convalida
Equipaggiare l’autoclave con una sonda centrale e posizionarla all’interno di un recipiente di riferimento. Questo ci permetterà di monitorare con precisione l’evoluzione della temperatura nel carico e di verificare che il carico sia stato esposto alla temperatura target per il tempo necessario. Si consiglia inoltre di utilizzare indicatori biologici e chimici per confermare la corretta sterilizzazione e di tenere un registro dettagliato di tutti i processi eseguiti.
-
Movimentazione del carico
Evitare di aprire prematuramente lo sportello dell’autoclave e maneggiare con cautela i contenitori una volta terminato il ciclo. Come abbiamo visto, i liquidi impiegano molto più tempo a riscaldarsi rispetto agli oggetti solidi e lo stesso accade durante la fase di raffreddamento.
-
Pulizia e manutenzione regolare dell’autoclave
Mantenere l’autoclave pulita ed eseguire ispezioni e manutenzioni regolari per garantire il corretto funzionamento dei meccanismi di sicurezza e prolungare la sua vita utile.
Seguendo queste pratiche, è possibile migliorare l’efficienza e la sicurezza della sterilizzazione dei liquidi in autoclave, garantendo risultati coerenti e affidabili in qualsiasi contesto.