El ciclo gravitatorio se ha consolidado como una metodología tradicional y ampliamente utilizada en la esterilización húmeda mediante autoclave. Su simplicidad, efectividad y bajo coste lo convierten en una opción atractiva para diversos entornos.
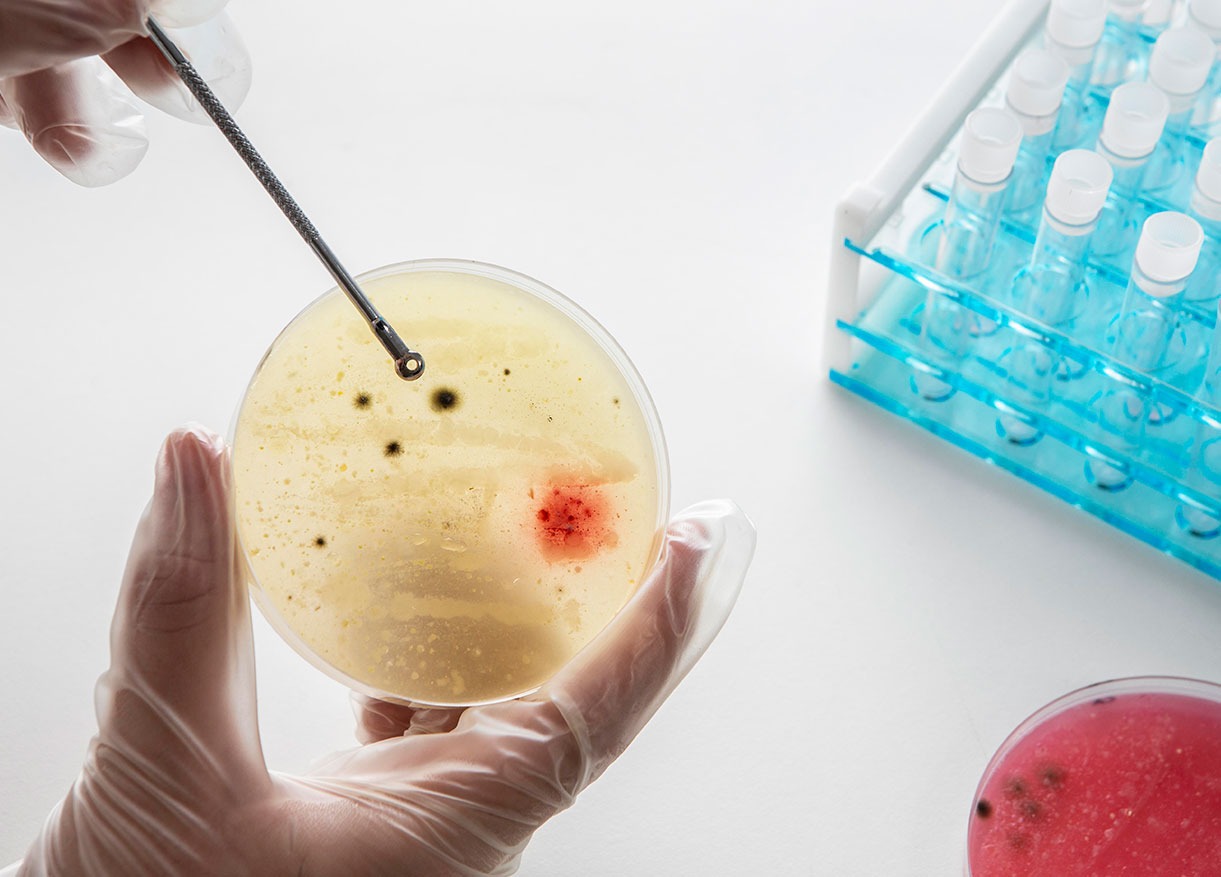
Este ciclo se caracteriza por su método de eliminación del aire de la cámara de esterilización: el vapor se genera en la parte inferior de la cámara y, tras calentar el aire en la parte inferior, este decrece en su densidad y es empujado hacía arriba y hacía el exterior. Tras varios minutos, la fracción de aire presente en la cámara se ha reducido notablemente y lo que queda principalmente es vapor de agua saturado.
Este proceso se basa en la ley de la gravedad, de aquí surge el término «gravitatorio». La eficiencia de este método radica en su simplicidad y en la capacidad del vapor presurizado para alcanzar altas temperaturas y transmitir muy eficazmente el calor a la carga, lo que le hace ideal para poder esterilizar eficazmente a bajo coste.
El ciclo gravitatorio es especialmente adecuado para materiales de geometrías sencillas, que no son sensibles a la humedad y que pueden soportar temperaturas superiores a los 121ºC, como lo son el vidrio, los metales y algunos plásticos. Es comúnmente utilizado en laboratorios de universidades, industrias, centros de investigación y entornos sanitarios para esterilizar instrumentos que no tienen cavidades internas o embalajes complejos.
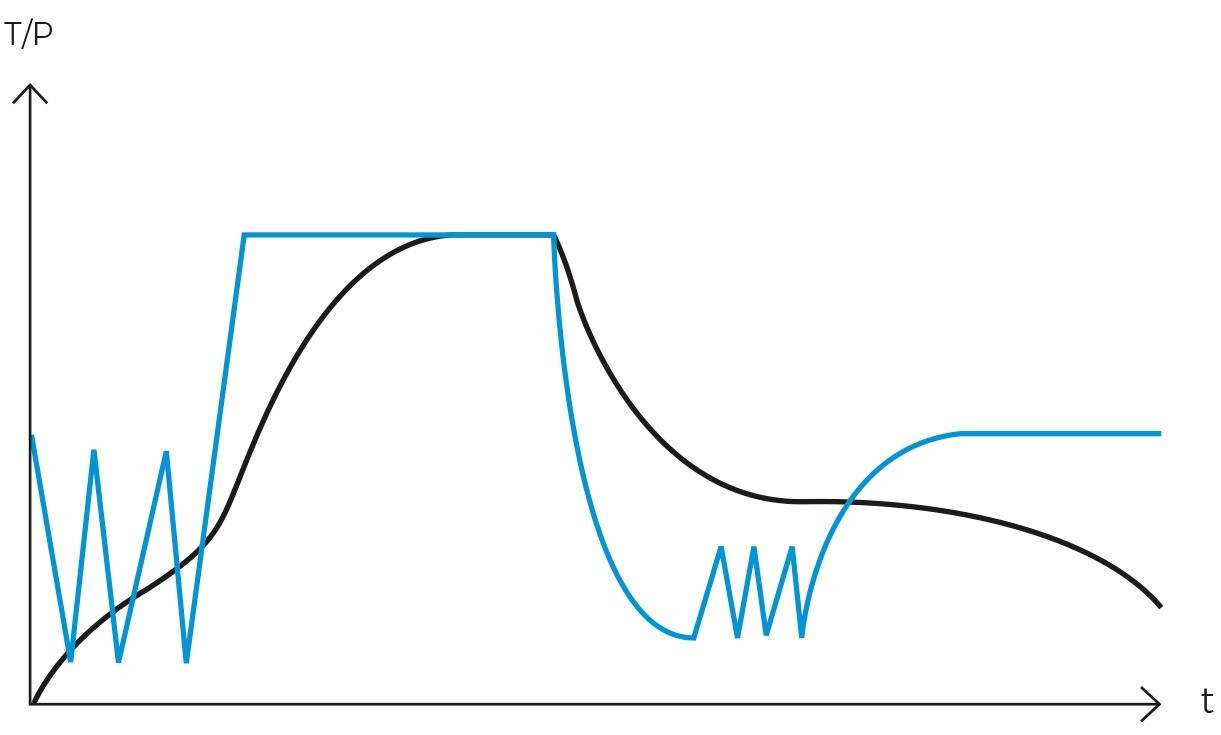
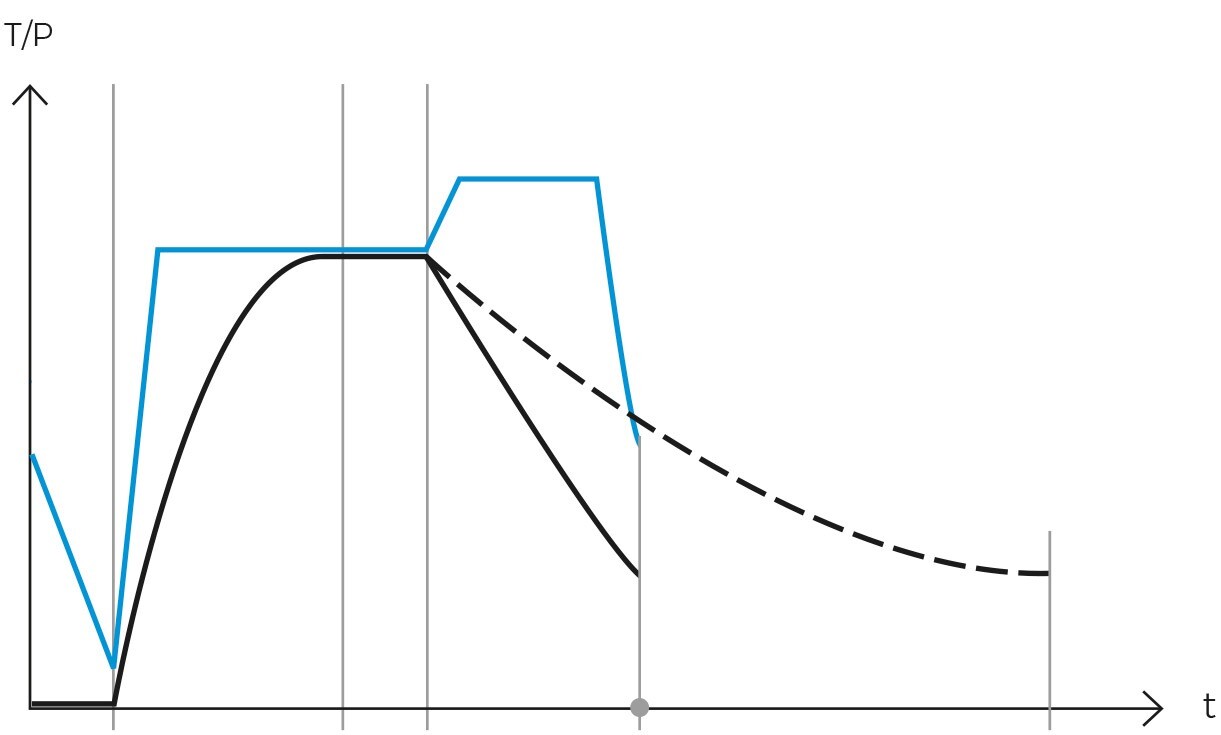
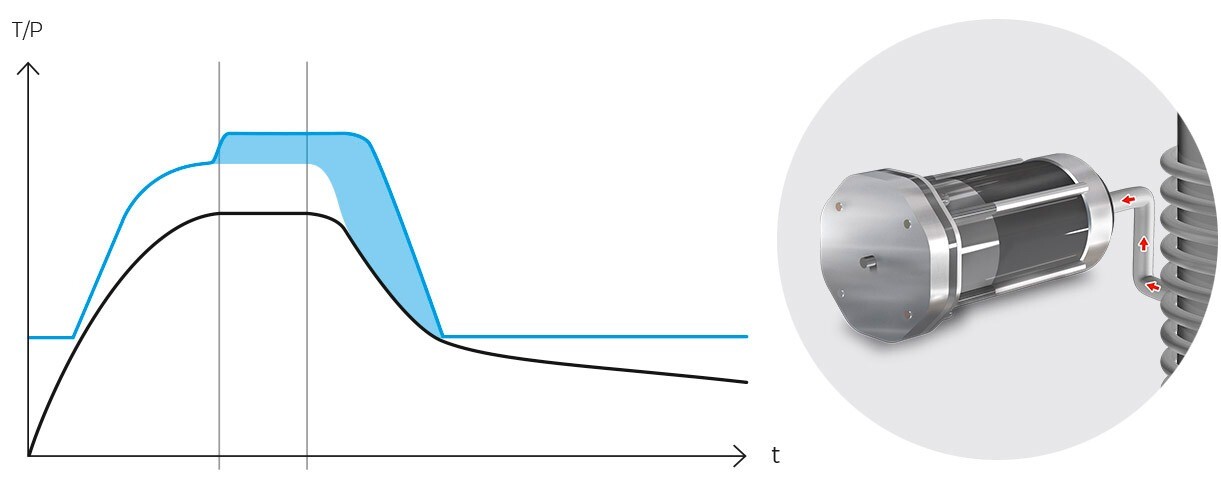
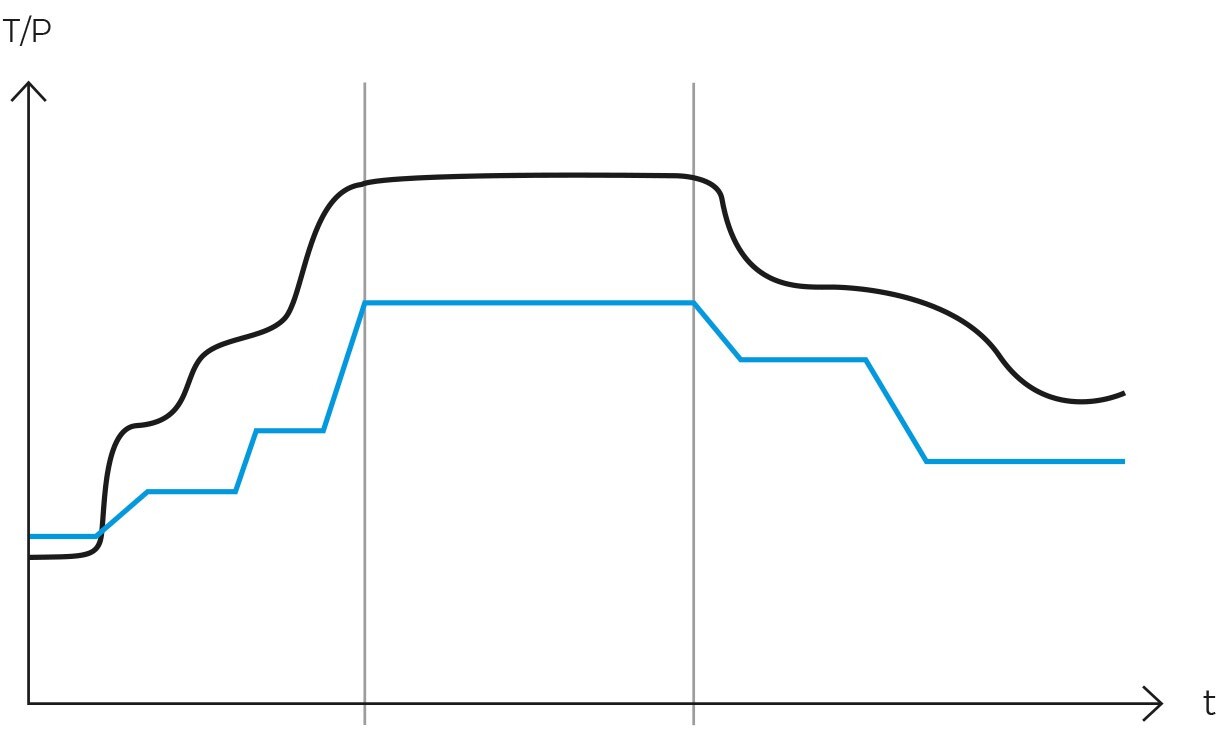
A nivel operativo, el ciclo gravitatorio suele seguir el siguiente patrón, donde primero se calienta la carga mientras se expulsa el aire frío al exterior, luego se cierra la válvula de purga y empieza a aumentar la presión interior hasta alcanzar la temperatura de esterilización. Entonces empieza la fase de esterilización y tras alcanzar el tiempo de exposición programado, comienza la fase de enfriamiento natural donde se enfriará y despresurizará la cámara y la carga progresivamente.
Una de las principales ventajas del ciclo gravitatorio es su simplicidad. No requiere de sistemas de vacío, ni compresor de aire, ni camisa calefactora, ni generador de vapor, ni de bombas adicionales, lo que permite que una autoclave que solo realiza este tipo de ciclos sea mucho menos costosa y su mantenimiento sea muy sencillo. Además, la eficacia de este tipo de ciclos para eliminar microorganismos ha sido ampliamente demostrada, lo que lo convierte en un método confiable para la esterilización de múltiples tipos de objetos.
Sin embargo, el ciclo gravitatorio tiene sus limitaciones. Por ejemplo, no es compatible con la esterilización de materiales porosos u objetos empaquetados. Esto es debido a que su sistema de eliminación de aire no es excelente, y el aire remanente en la cámara actúa como aislante impidiendo que el vapor pueda penetrar adecuadamente en todas las superficies de la carga. Tampoco sirve para esterilizar objetos sellados herméticamente. En estos casos, se pueden considerar otros métodos de esterilización, como el ciclo de vacío o el ciclo con contrapresión.
Principios de funcionamiento del ciclo gravitatorio
El ciclo gravitatorio en una autoclave se distingue por su eficiencia y simplicidad, fundamentándose en el uso de vapor de agua a alta presión y alta temperatura. A continuación, detallamos los principios clave que rigen su funcionamiento:

-
Generación y uso del vapor de agua
La autoclave calienta el agua hasta convertirla en vapor saturado, es decir, vapor que no contiene gotas de agua en suspensión. Este vapor va accediendo a todos los rincones de la cámara de la esterilización, proporcionando una transferencia de calor eficiente y uniforme. En las autoclaves más sencillas, la generación de vapor se realiza mediante resistencias eléctricas situadas en la base de la autoclave. En las autoclaves más avanzadas, es un generador de vapor situado fuera de la cámara el que inyecta vapor saturado al interior de la cámara de esterilización.
-
Purga, expulsión del aire
El vapor caliente, más ligero que el aire, se eleva y desplaza el aire hacia el exterior de la cámara a través de una válvula de purga que se encuentra abierta durante este paso. Este proceso, basado en la ley de la gravedad, es crucial para eliminar el aire de la cámara, ya que la presencia de bolsas de aire frío impide que el vapor entre en contacto con todas las superficies de los objetos a esterilizar.
-
Fase de esterilización
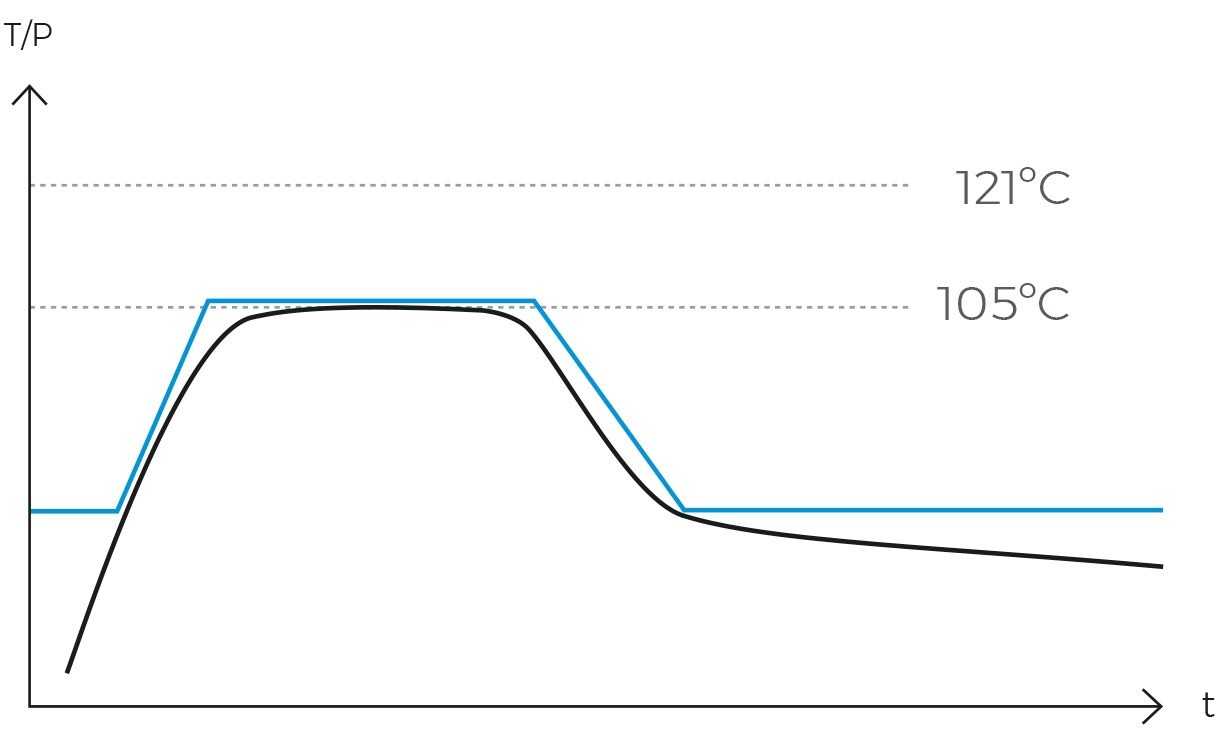
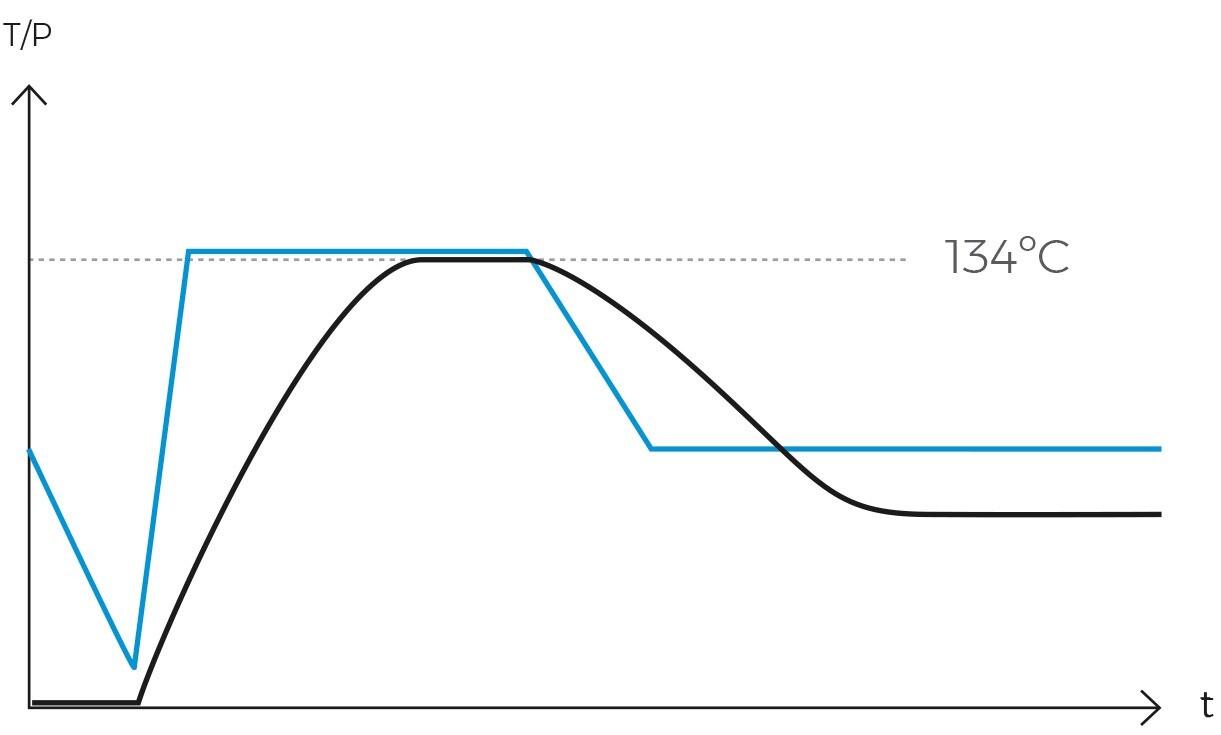
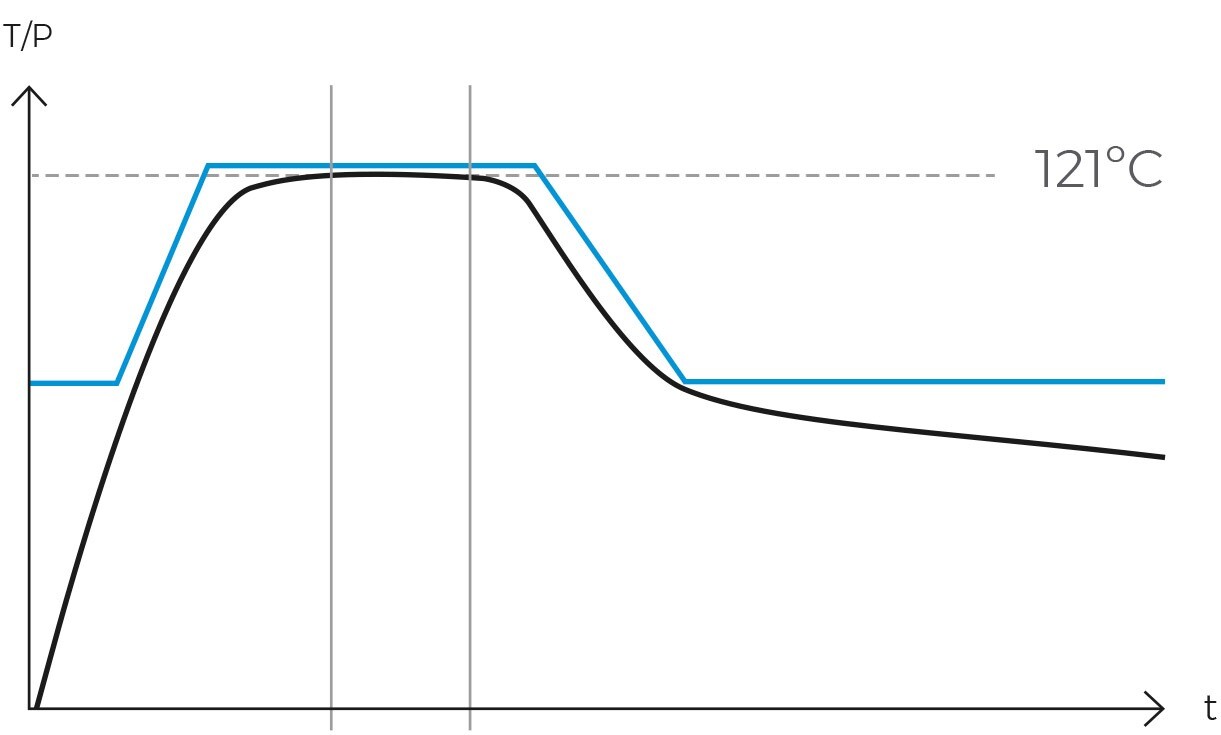
Una vez que el aire ha sido expulsado completamente, la cámara se sella y la temperatura del vapor sigue subiendo hasta alcanzar la temperatura de esterilización, que suele ser de 121ºC. En ese momento se mantendrá constante y sin fluctuaciones la temperatura y la presión durante un período determinado. Esta combinación de temperatura, presión y tiempo asegura la completa transmisión de energía del vapor hacía la carga, inactivando todos los microorganismos. La duración de esta fase varía según el tipo de material a esterilizar y la carga microbiana presente.
-
Enfriamiento y finalización del ciclo
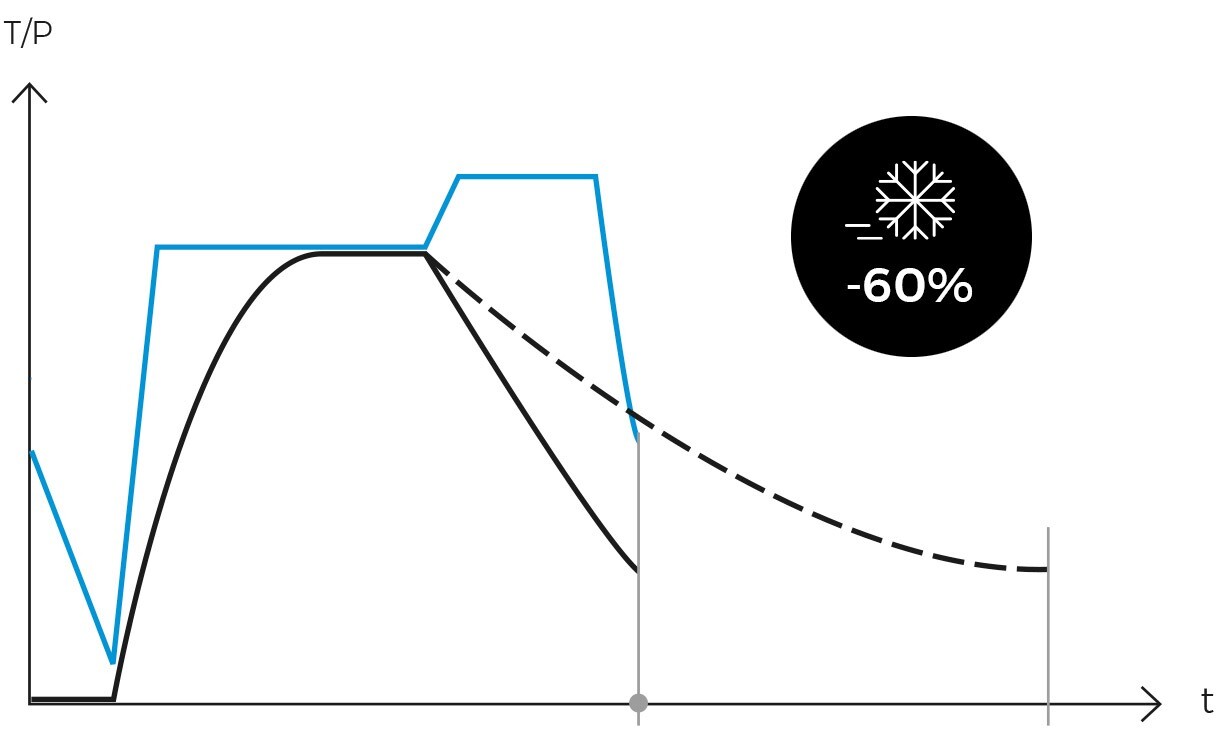
Tras la esterilización, se inicia la fase de enfriado. El vapor se libera de la cámara, reduciendo la presión de manera controlada y permitiendo que los artículos se enfríen. En los programas de sólidos este paso tiene lugar a gran velocidad mientras que en las autoclaves que cuentan con programas de líquidos este paso se debe realizar a menor velocidad y de forma escalonada para evitar salpicaduras o roturas de recipientes debido a un cambio brusco de temperatura y presión.
En caso de tratarse de cargas sólidas, nuestra autoclaves de la Serie AES incorporan un pulsador que permite liberar rápidamente al exterior el vapor ubicado en el interior de la cámara una vez finalizado el ciclo de esterilización. En cambio, otros modelos más avanzados realizan este procedimiento de forma automática en los programas de sólidos e incluso cuenta con sistemas de secado para garantizar que los materiales esterilizados salgan secos y listos para su uso o almacenamiento.

-
Control y monitoreo
Durante todo el ciclo, es esencial un control riguroso de los parámetros de tiempo, temperatura y presión. Nuestras autoclaves están equipadas con sistemas de monitoreo y control automáticos que garantizan la precisión y reproducibilidad del proceso. También pueden equiparse con impresoras de tickets y software de gestión, permitiendo un control absoluto de todos procesos realizados en la autoclave.
Ciclo gravitatorio vs ciclo de vacío
La elección entre el ciclo gravitatorio y el ciclo de vacío en autoclaves depende de las necesidades específicas de esterilización del laboratorio donde se ubicará la autoclave. Aunque una autoclave de vacío puede realizar un ciclo gravitatorio, una autoclave económica diseñada exclusivamente para ciclos gravitatorios nunca podrá realizar un ciclo de vacío. Por ello, es crucial elegir el modelo adecuado de autoclave en el momento de la compra, teniendo en cuenta el uso actual y futuro que se requerirá.
Ciclo gravitatorio
El ciclo gravitatorio está indicado para la esterilización de objetos sólidos, instrumentos, líquidos, materiales no porosos y cargas no embolsadas. Este ciclo se utiliza comúnmente en laboratorios, universidades, escuelas y centros de investigación para esterilizar cristalería e instrumentos sencillos que no poseen cavidades internas o geometrías complejas. Su principal ventaja radica en un menor coste de adquisición, mantenimiento y operación, gracias a su simplicidad.
Ciclo de vacío
Por otro lado, el ciclo de vacío implica crear un vacío dentro de la cámara antes de introducir el vapor. Este proceso elimina de manera efectiva todas las bolsas de aire presentes en materiales porosos o en objetos con cavidades internas, lo que lo hace adecuado para la esterilización de materiales más complejos, como bolsas de residuos, instrumentos quirúrgicos con lúmenes, textiles, objetos embolsados y biorreactores. Su principal ventaja radica en proporcionar una esterilización eficaz para cargas más desafiantes.
¿Qué ciclo es más eficiente?
En términos de eficiencia, el ciclo de vacío supera al ciclo gravitatorio en la esterilización de objetos con superficies difíciles de penetrar o materiales porosos. Sin embargo, el ciclo gravitatorio es más rápido, rentable y suficientemente eficaz para cargas simples y no porosas.
Desde el punto de vista de costes y mantenimiento, las autoclaves que operan con ciclos de vacío son más costosas y requieren un mantenimiento más frecuente y riguroso debido a sus componentes, que pueden incluir un sistema de vacío, un compresor de aire, una camisa calefactora, un filtro bacteriológico, un sistema de enfriado rápido o un generador de vapor. Además, para operar requieren un sistema de purificación de agua.
Aplicaciones del ciclo de gravedad
El ciclo gravitatorio con autoclave, conocido por su popularidad y simplicidad, se utiliza en una amplia variedad de sectores. A continuación, se detallan algunas de las aplicaciones más comunes de este ciclo, presentadas de manera concisa y clara:
-
Laboratorios de investigación y ciencias de la vida
En estos laboratorios, el ciclo gravitatorio se emplea para esterilizar medios de cultivo, soluciones acuosas, instrumentos metálicos y cristalería de laboratorio. Es particularmente adecuado para la esterilización rutinaria de pipetas, matraces y otros recipientes de vidrio.

-
Laboratorios de control de calidad en la industria alimentaria y de bebidas
Para el control de calidad en la industria alimentaria, se suele emplear el ciclo gravitacional en la esterilización de instrumentos, objetos de vidrio, medios de cultivo, desechos de laboratorio y contenedores. La correcta esterilización de la carga es fundamental para prevenir la contaminación y asegurar la seguridad alimentaria de la producción, ayudando así a mantener los estándares de higiene y calidad en toda la industria.
-
Plantas de tratamiento de aguas residuales
En cualquier laboratorio de una planta de tratamiento de aguas se debe realizar un control preciso de la contaminación microbiológica de las aguas residuales y las aguas tratadas. En estos centros se utiliza el ciclo gravitatorio para esterilizar soluciones, cristalería de laboratorio, medios de cultivo y soluciones. Es particularmente adecuado para la esterilización rutinaria de tubos de ensayo, placas de Petri, embudos, buretas y botellas con líquidos.
-
Centros educativos y universidades
En este sector las autoclaves generalmente están equipadas exclusivamente con la funcionalidad para llevar a cabo el ciclo gravitatorio, y su uso es ampliamente extendido debido a su coste-eficiencia y confiabilidad. Estos dispositivos son populares no solo por poder esterilizar cargas líquidas acuosas y medios de cultivo de manera efectiva sino también por poder procesar una amplia variedad de materiales sólidos, como matraces, puntas de pipeta, botellas de vidrio y placas de Petri.
-
Industria farmacéutica, biotecnológica y cosmética
En este sector suele tener preferencia por el empleo de ciclos de vacío y ciclos con soporte de presión, especialmente para la producción de productos farmacéuticos y biotecnológicos envasados en recipientes. No obstante, el ciclo gravitatorio se utiliza para esterilizar líquidos y objetos de vidrio.
-
En el ámbito clínico
Este ciclo se utiliza habitualmente en laboratorios de hospitales, clínicas y centros sanitarios para procesar cargas sencillas y no embolsadas. Es ideal para esterilizar instrumentos metálicos como bandejas, tijeras, pinzas y otros utensilios de acero inoxidable. Proporciona una esterilización efectiva y rápida, esencial para mantener un alto nivel de cuidado y prevención de infecciones. No obstante, para procesar objetos más delicados como instrumental laparoscópico o implantes médicos se usa siempre un ciclo de vacío.
-
Veterinaria y cuidado de animales
Igual que en el ámbito clínico, el ciclo gravitatorio también se aplica en hospitales veterinarios y centros de cuidado animal para esterilizar cargas sencillas y no embolsadas. Esto permite minimizar el riesgo de transmisión de enfermedades entre animales y entre animales y humanos.
Factores críticos para garantizar la eficacia del ciclo gravitatorio
Para garantizar la eficacia del ciclo gravitatorio en la esterilización en autoclave, es crucial considerar y controlar varios factores. Estos factores son fundamentales para asegurar un proceso de esterilización efectivo y seguro:
-
Carga y distribución de los materiales
La manera en que se cargan los materiales en la autoclave tiene un impacto significativo en la eficacia del ciclo. Es importante distribuir los objetos de manera uniforme y asegurarse de que no estén demasiado apretados o apilados, para permitir una circulación adecuada del vapor.
-
Correcta eliminación del aire
La eficiencia del ciclo gravitatorio depende en gran medida de la eliminación completa del aire de la cámara de esterilización. Si queda aire residual, puede impedir que el vapor saturado alcance todas las superficies de los objetos a esterilizar, lo que podría resultar en una esterilización incompleta. Por ello debe revisarse que la purga se realice correctamente y la válvula de purga esté libre de obstrucciones.
-
Control riguroso de la esterilización
Es vital mantener la temperatura y la presión adecuadas durante el ciclo de esterilización. Generalmente, se requiere alcanzar y mantener una temperatura de al menos 121°C a una presión específica para asegurar la eliminación efectiva de todos los microorganismos. Para ello debe registrarse y comprobarse los resultados de cada ciclo y además debe acompañarse del uso de elementos de control biológico y/o químico que validen la correcta esterilización de la carga. Entre ellos podemos mencionar la cinta de control de esterilización o el test de esporas.
-
Tiempo de exposición adecuado
El tiempo durante el cual los materiales están expuestos al vapor saturado debe ser suficiente para garantizar una eliminación correcta. Este tiempo de exposición varía en función del tipo de material que se esteriliza y de la carga microbiana presente. Por lo que deberá revisarse con el fabricante que los parámetros de cada programas sean los adecuados. Como regla general, es mejor optar siempre por la cautela y alargar el tiempo de esterilización en caso de duda.
-
Mantenimiento y calibración de la autoclave
El mantenimiento regular y la calibración adecuada de la autoclave son cruciales para su funcionamiento óptimo. Esto incluye la verificación periódica de componentes críticos como sellos, válvulas y sensores, así como la calibración precisa de los controles de temperatura y presión. La exactitud y precisión de las sondas de temperatura que rigen el ciclo de esterilización de la autoclave pueden degradarse con el tiempo de forma que hay que verificar periódicamente que funcionan perfectamente.
Consideraciones de seguridad y mantenimiento
La operación segura y el mantenimiento adecuado de las autoclaves con ciclo gravitatorio son esenciales para prevenir riesgos y garantizar la eficiencia del proceso de esterilización. A continuación, presentamos algunas consideraciones clave en estos aspectos:
Seguridad de los operarios
La operación de la autoclave debe seguir estrictamente las instrucciones del fabricante y las normativas de seguridad. Los operadores deben estar capacitados en el uso del equipo y conscientes de los riesgos asociados a trabajar con maquinaria que opera con vapor a alta presión y temperatura. Es crucial evitar la apertura de la autoclave durante su funcionamiento para prevenir la liberación repentina de vapor caliente y presurizado. Si bien las autoclaves modernas cuentan con sistemas de bloqueo de puerta mientras el ciclo está en marcha, al finalizar el programa y abrir la puerta la carga puede aún estar muy caliente, especialmente las cargas líquidas voluminosas.
Mantenimiento preventivo
Implementar un programa de mantenimiento preventivo es esencial para el funcionamiento óptimo y seguro de la autoclave. Esto incluye inspecciones regulares de componentes de seguridad críticos como las juntas, válvulas, filtros y sensores, así como la sustitución inmediata de piezas que estén desgastadas.
Calibración y comprobaciones periódicas
La calibración regular de los controles de temperatura y presión es vital para asegurar que la autoclave funciona correctamente. Además, realizar comprobaciones periódicas de la eficacia de cada ciclo con cinta de control de esterilización o test de esporas es recomendable para verificar la eficacia del proceso de esterilización en cada rotación.
Empleo de agua limpia
Es vital renovar periódicamente el agua usada y solo usar agua destilada o purificada para evitar la transferencia de sales a la carga y la formación de depósitos de sales en las paredes y cubierta interior de la cámara de esterilización con el paso del tiempo.
Limpieza y desinfección
Es importante limpiar y desinfectar regularmente la cámara de esterilización y otras partes de la autoclave para evitar la acumulación de residuos, formación de depósitos de sales y prevenir la contaminación cruzada. Se deben seguir las recomendaciones del fabricante en cuanto a los agentes de limpieza y desinfección adecuados.

Manejo de materiales esterilizados
Después de la esterilización, los materiales deben manejarse con cuidado para preservar su esterilidad. Esto incluye permitir que los artículos se enfríen adecuadamente antes de manipularlos y almacenarlos en un entorno limpio y seco. En el caso de no contar con una autoclave con secado, deberá usarse una estufa de laboratorio para secar la carga sólida antes de usarse.
Registro y documentación
Es crucial mantener un registro detallado de los ciclos de esterilización, los mantenimientos realizados y cualquier incidencia para facilitar el control de calidad del equipo. Estos registros son también fundamentales para cumplir con las normativas y estándares de calidad como las buenas prácticas de laboratorio (GLP).